Weltweit nehmen die Bemühungen zu, gentechnisch veränderte Pflanzen ebenso wie bisher z.B. Bakterien oder Hefen als Produktionsorganismen für Impfstoffe und andere pharmazeutisch wirksame Substanzen zu nutzen. In den USA und Kanada, verstärkt aber auch in Europa und hier vor allem in Frankreich, werden solche Pflanzen in Freisetzungsversuchen getestet und daraus gewonnene Arzneimittel bereits klinisch geprüft. Für die Biologische Sicherheit ergeben sich beim Anbau von Pharmapflanzen völlig neue Anforderungen.
Die Produktion von Arzneimitteln mit Hilfe gentechnischer Methoden ist nicht neu, sie beschränkte sich aber bislang auf die Produktion in geschlossenen Systemen auf Basis mikrobieller, sowie tierischer und selten auch pflanzlicher Zellen bzw. Gewebe (Fermenter- oder Bioreaktorproduktion). Diese Arzneimittel, so genannte Biopharmazeutika, werden produziert, indem die Gene, die für den gewünschten Stoff codieren, in den Produktionsorganismus eingebracht werden und dort exprimieren. Insbesondere das Bakterium Escherichia coli kommt dabei zum Einsatz. Knapp zwei Drittel der zugelassenen gentechnisch erzeugten Arzneimittel, so auch das erste bereits 1982 erzeugte rekombinante Arzneimittel, menschliches Insulin, werden in E.coli produziert.
Sieben der 50 umsatzstärksten Arzneimittel waren 2003 Biopharmazeutika. Sie machen derzeit etwa sieben Prozent des Arzneimittelweltmarktes aus.
Durch geeignete gentechnische Modifikationen können auch Pflanzen als Produktionsorganismen für Biopharmazeutika genutzt werden. Dabei werden die in der Pflanze produzierten pharmazeutischen Stoffe anschließend extrahiert und aufgereinigt. Ansätze, impfstoffhaltige Pflanzen zu entwickeln, die durch Verzehr der Pflanze selbst einen Impfschutz bewirken, sind zwar in der Diskussion, aber noch weit entfernt von einer realistischen Perspektive.
Freisetzungen von Pharmapflanzen
Bis Ende 2003 wurden in den USA, Kanada und der EU insgesamt 186 Anträge auf Freisetzungen mit PMP produzierenden Pflanzen gestellt, davon die ersten in den USA bereits 1991.
In Deutschland wurde 2006 eine erste Freisetzung mit Pharmapflanzen genehmigt. Wissenschaftler der Universität Rostock wollen über mehrere Jahre untersuchen, inwieweit sich Kartoffeln als Produktionssystem für Impfstoffe eignen.
Die für die Freisetzungen verwendeten Nutzpflanzen sind hauptsächlich Mais und Tabak, gefolgt von Raps und Soja. Pharmastoffe, die aus ihnen gewonnen werden, sind Blut- und Blutgerinnungsproteine, Impfstoffe, Gerüstsubstanzen wie Kollagen, antimikrobielle oder antivirale Wirkstoffe, Wachstumshormone verschiedene Enzyme sowie insbesondere Antikörper. Diese sind bisher am intensivsten in pflanzlichen Produktionssystemen untersucht worden. Therapeutische Antikörper etwa zur Behandlung von Krebs, Autoimmunerkrankungen und Infektionskrankheiten bilden einen Schwerpunkt bei der Entwicklung von PMP.
Noch keine PMP produzierende Pflanze zugelassen
Die ersten in transgenen Pflanzen produzierten pharmazeutischen Wirkstoffe befinden sich bereits in verschiedenen Phasen klinischer Prüfungen. Bislang gibt es aber weltweit noch keine Zulassung für eine PMP produzierende Pflanze. Es sind lediglich einige Proteine (z.B. Trypsin aus Mais, Lactoferrin aus Reis) kommerziell erhältlich, die aus experimentellen Freisetzungen (USA) stammen und für Forschung bzw. Diagnostik verwendet werden dürfen.
In den USA wurde Anfang 2006 ein erstes Plant made Pharmaceutical, ein von der Firma Dow AgroSciences hergestellter Impfstoff für Tiere, zugelassen. Dieses Arzneimittel wurde auf der Basis pflanzlicher Zellkulturen produziert.
Die intensivste Forschung und Entwicklung zu PMP findet in den USA und Kanada statt. Aber auch europäische Firmen haben die Nase vorn. So befindet sich ein PMP der französischen Firma Meristem therapeutics zur Behandlung von Mukoviszidose in der Entwicklung. Dieses PMP, eine gastrische Lipase, wird in Mais gebildet und ist bereits in experimentellen Freisetzungen getestet worden. Es könnte das erste Medikament aus gv-Pflanzen sein, für das in Europa eine Zulassung beantragt wird. Diesem PMP wurde 2003 der so genannte Orphan-Drug-Status zuerkannt. Das bedeutet, dem Unternehmen wird im Falle einer erfolgreichen Zulassung garantiert, dass das Medikament bis zu zehn Jahre auf dem Markt exklusiv bleibt. Diesen Status hat im selben Jahr in den USA ein weiteres PMP zuerkannt bekommen.
Als mögliche Vorteile von Pflanzen gegenüber anderen Produktionssystemen werden in der Diskussion vor allem folgende Argumente angeführt: Die Produktion auch großer Mengen pharmazeutischer Wirkstoffe könnte durch den Freilandanbau flexibler und kostengünstiger an die Markterfordernisse angepasst werden; eine Verunreinigung durch Humanpathogene, den Menschen betreffende Krankheitserreger, ließe sich vermeiden; da Proteinstrukturen sich im Produktionsorganismus verändern und damit einen Einfluss auf die gewünschten Eigenschaften der gebildeten Stoffe haben, sind möglicherweise Pflanzenzellen geeigneter für die Produktion, weil sie den menschlichen Zellen ähnlicher sind als etwa Bakterien.
Herausforderung für die Biologische Sicherheit
Pflanzen, die veränderte Inhaltsstoffe und pharmazeutisch wirksame Substanzen bilden, stellen völlig neue Anforderungen an die Sicherheit. Anders als gv-Pflanzen der ersten Generation, die v.a. Wirkstoffe gegen Fraßinsekten bilden oder resistent gegenüber bestimmten Herbiziden sind, werden mit Hilfe von Pharmapflanzen gezielt Stoffe produziert, die eine Wirkung auf Menschen oder höhere Tiere haben. Sie werden darüber hinaus optimiert hinsichtlich der Wirkstoff-Erträge, d.h. sie produzieren ein Vielfaches der Wirkstoffmengen im Vergleich mit bisherigen gv-Pflanzen, und es werden oftmals mehrere genetische Modifikationen gleichzeitig vorgenommen, etwa um die Pflanzen aus Sicherheitsgründen steril zu machen, mit einer entsprechend höheren Wahrscheinlichkeit für unerwartete Effekte.
2002 entbrannte in den USA die Diskussion um die Risiken freigesetzter Pharmapflanzen, als Reste gentechnisch veränderter Maispflanzen in Sojabohnen gefunden wurden. Die texanische Biotechnologiefirma ProdiGene, eines der führenden Unternehmen bei der Entwicklung von PMP, hatte gentechnisch veränderten Mais freigesetzt, der Trypsin, ein Protein der Bauchspeicheldrüse bildet. Trypsin wird u.a. zur Herstellung von Insulin verwendet. Nach Abschluss des Versuchs wurde auf dem Feld Soja für den menschlichen Verzehr angepflanzt. Bei Überprüfung der geernteten Sojabohnen fanden sich Reste von Mais. ProdiGene musste die Ernte von rund 13500 Tonnen Sojabohnen im Wert von zwei Millionen Dollar ankaufen und vernichten sowie zusätzlich eine Strafe zahlen.
Der Konflikt um den Trypsin-Mais hatte deutlich gemacht, dass Arzneimittel produzierende Pflanzen besondere Sicherheitsmaßnahmen erfordern, um sie strikt von Lebens- und Futtermittelpflanzen zu trennen. Neben verschiedenen Maßnahmen, solche Pflanzen physikalisch oder auch biologisch “einzuschließen”, wäre auch die Verwendung von Non-Food-Pflanzen eine Möglichkeit, Risiken einzugrenzen. Allerdings sind für viele PMP-Projekte in den USA bislang immer noch Mais, Raps, Reis oder Kartoffeln die Pflanzen der Wahl.
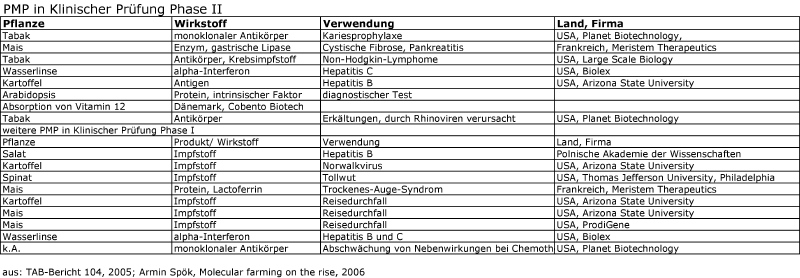
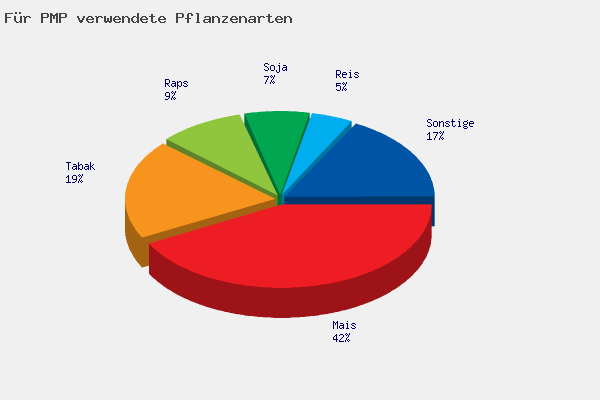
Die wichtigsten für PMP verwendeten Pflanzenarten. In den USA wird vor allem Mais zur Produktion von PMP eingesetzt, in Kanada und der EU dagegen hauptsächlich Pflanzen, die keine Nahrungsmittel liefern, wie Tabak.
(aus: TAB-Bericht 104)
(Vgl. Meldungen vom 2007-01-21 und 2006-04-20.)
Source
bioSicherheit.de, 2007-02-19.
Share
Renewable Carbon News – Daily Newsletter
Subscribe to our daily email newsletter – the world's leading newsletter on renewable materials and chemicals









