Wissenschaftler am Max-Planck-Institut für Dynamik komplexer technischer Systeme Magdeburg haben mit Hilfe neu entwickelter Computeralgorithmen fünf der wichtigsten biotechnologischen Produktionsorganismen wie Escherichia coli und Bäckerhefe daraufhin analysiert, wie sich das Wachstum der Zellen optimal mit der Überproduktion von (Bio-)Chemikalien koppeln lässt. In ihren Berechnungen zeigten sie, dass für fast jedes Stoffwechselprodukt in den untersuchten Organismen geeignete genetische Interventionen existieren, mit denen eine Kopplung der Synthese des Produkts mit Zellwachstum möglich ist. Die Ergebnisse der Studie tragen grundlegend zur Entwicklung von neuen biotechnologischen Prozessen bei.
![Dr. Oliver Hädicke aus der Arbeitsgruppe Analyse und Redesign biologischer Netzwerke untersucht ein bakterielles Stoffwechselnetzwerk am Computer. Wissenschaftler des Max-Planck-Instituts für Dynamik komplexer technischer Systeme Magdeburg haben zu diesem Zweck die Software CellNetAnalyzer entwickelt. [weniger] © Max-Planck-Institut Magdeburg](https://renewable-carbon.eu/news/wp-content/uploads/2017/08/zoom2-300x225.jpg)
© Max-Planck-Institut Magdeburg
Der Stoffwechsel (Metabolismus) selbst eines recht einfachen Mikroorganismus ist hochgradig komplex und umfasst in der Regel Hunderte oder gar Tausende Metabolite (wie Zucker oder organische Säuren) und biochemische Reaktionen. Um im Labyrinth der sich daraus ergebenden Stoffwechselnetzwerke nicht den Überblick zu verlieren, verwenden Wissenschaftler neben Laborexperimenten verstärkt mathematische Modelle und Computersimulationen. Diese helfen unter anderem bei der Suche nach Kombinationen von genetischen Eingriffen, die eine normale Zelle in eine biochemische Fabrik zur Synthese eines gewünschten Produktes umwandeln.
Im Idealfall lässt sich dabei das Wachstum der Zelle obligatorisch mit der Synthese des Produkts koppeln. Die Zelle kann sich dann nämlich nur noch vermehren, wenn die gewünschte Chemikalie als Nebenprodukt entsteht. Eine solche Kopplung läuft zum Beispiel in natürlicher Art und Weise ab, wenn Hefen unter Sauerstoffausschluss das Gärprodukt Alkohol produzieren (müssen). Da Mikroorganismen gewöhnlich immer nach maximalem Wachstum streben, vereinen die Ingenieure dadurch geschickt ihre Interessen mit denen des Lebewesens. Für bestimmte Produkte wurde in konkreten Beispielen gezeigt, dass eine solche Kopplung erzwungen werden kann. Bisher war aber unklar, inwieweit sich dieses Prinzip auf ein breites Spektrum von anderen Produktklassen und für verschiedene Mikroorganismen verallgemeinern und anwenden lässt.
Wachstumsgekoppelte Überproduktion ist fast universell möglich
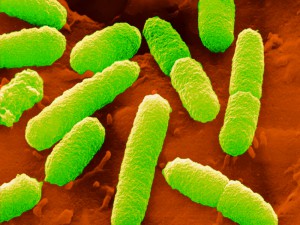
Mikroskopaufnahme von Escherichia coli
© Mit freundlicher Genehmigung: Jürgen Berger / MPI für Entwicklungsbiologie
Dieser Frage sind nun Wissenschaftler der Arbeitsgruppe „Analyse und Redesign biologischer Netzwerke“ am Max-Planck-Institut in Magdeburg unter der Leitung von Dr. Steffen Klamt auf den Grund gegangen. Die Forscher untersuchten für fünf der wichtigsten biotechnologischen Produktionsorganismen (einschließlich der häufig verwendeten Arbeitspferde Escherichia coli und Bäckerhefe, aber auch andere wie zum Beispiel photosynthetische Bakterien), für welche Metabolite eine mit Wachstum gekoppelte Synthese möglich ist. Für diese aufwändigen Berechnungen entwickelten sie zunächst effiziente Algorithmen. Als zentrales und zugleich überraschendes Ergebnis zeigten sie damit schließlich, dass sich für fast jeden Metaboliten (>94%) in den fünf Modellorganismen eine Interventionsstrategie finden lässt, die Wachstum an eine Überproduktion des Metaboliten mit einer guten Ausbeute erzwingt. Die fünf Organismen decken ein breites Spektrum von relevanten Produkten für die chemische Industrie ab (wie zum Beispiel Biokraftstoffe, Biopolymere, Nahrungsergänzungsmittel oder Plattformchemikalien zur Synthese anderer Substanzen). Somit sind diese Ergebnisse, die in der Zeitschrift Nature Communications veröffentlicht wurden, von weitreichender Bedeutung für die Entwicklung neuer biotechnologischer Prozesse.
Unter Anwendung der oben beschriebene Kopplungsstrategie hatte die Gruppe jüngst in einer Parallelstudie einen Stamm des Bakteriums Escherichia coli mittels computergestützter Berechnungen erfolgreich so verändert, dass dieser Itaconsäure, eine wichtige Plattformchemikalie, mit bisher unerreichter Ausbeute aus Traubenzucker produziert. Dieses konkrete Anwendungsbeispiel hat das Potenzial der Kopplungsstrategie nochmals nachhaltig demonstriert.
Für weitere Forschungen zur computergestützten Optimierung des Stoffwechsels von Mikroorganismen wird die Gruppe um Steffen Klamt in den nächsten fünf Jahren mit zwei Millionen Euro durch den Europäischen Forschungsrat (European Research Council, ERC) gefördert.
Source
Supplier
European Research Council
Max-Planck-Institut für Dynamik komplexer technischer Systeme
Share
Renewable Carbon News – Daily Newsletter
Subscribe to our daily email newsletter – the world's leading newsletter on renewable materials and chemicals









